诺峰药业成都生产基地顺利获得FDA cGMP认证,全球合作再添里程碑
2025-08-2715:28
2025年8月20日,诺峰药业(Zennova Pharmaceuticals)宣布成都制剂生产中心成功通过美国食品药品监督管理局(FDA)的现行药品生产质量管理规范(cGMP)现场核查,并于日前正式获得FDA签发的《设施检查报告》(Establishment Inspection Report, EIR)。该报告确认成都生产基地完全符合FDA cGMP标准,标志着诺峰药业的质量管理体系和国际化运营能力再获权威认可。
此次FDA现场检查于2025年3月17日至22日进行,涵盖生产管理、质量控制、文件体系和现场操作等全流程。FDA的EIR认证是全球医药行业合规性与产品质量的权威背书,也是诺峰药业继两周内连续通过FDA及四川省药监局双重核查后的又一重大突破。
l质量第一,铸就全球信赖
诺峰药业董事长兼CEO郭大海表示:“我们非常自豪能够获得FDA的EIR认证。这不仅是对成都团队专业能力和严谨作风的高度认可,也体现了诺峰药业‘质量第一’核心价值观在全球实践中的扎实落地。此次通过FDA审核,进一步夯实了我们为全球合作伙伴提供合规、可靠、高质量药品的承诺。
”
l全球合作,助力中国企业出海
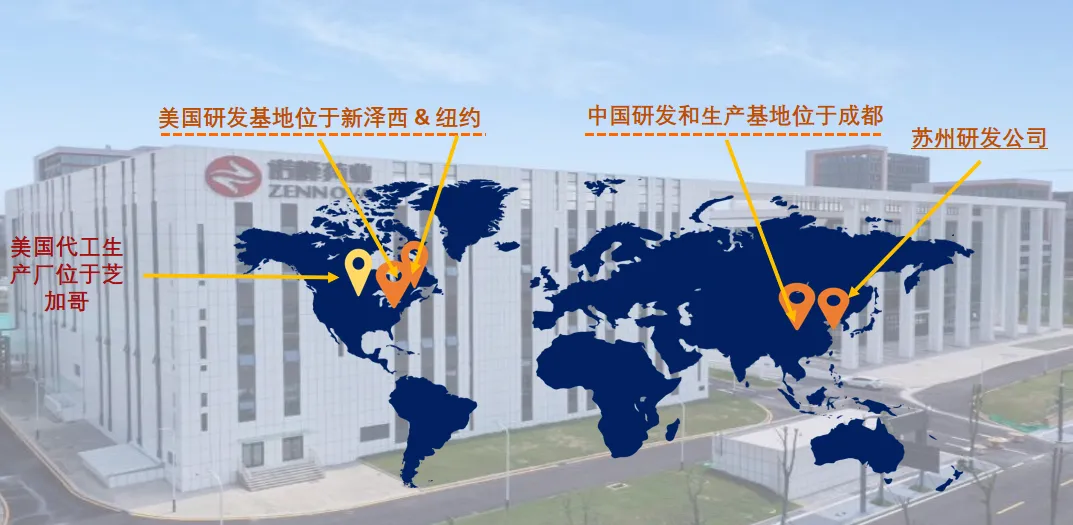
成都制剂生产中心作为诺峰药业的核心战略生产基地,承担着关键制剂研发与国际化生产的重要职能。此次认证将显著增强公司在创新药研发、生产、技术转移、国际注册和跨境CRDMO(合同研发与生产)等领域的服务能力,为国内外合作伙伴提供符合全球标准的一体化解决方案。
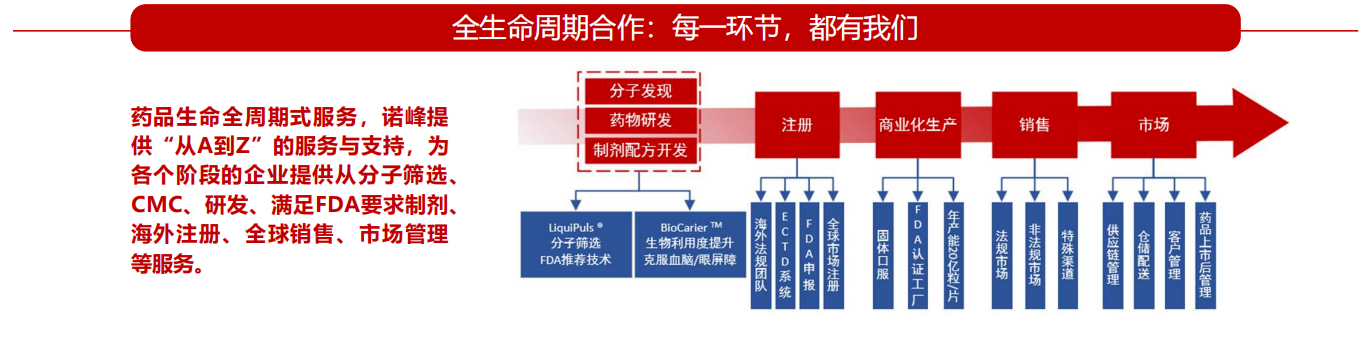
目前,诺峰药业已与多家中国及海外医药企业达成合作,依托其严格的质量体系和国际合规经验,成功推动多个药品研发与出海项目。公司近期签署多项海外订单,业务涵盖制剂开发、cGMP生产、国际注册及市场准入支持等服务,持续助力中国医药企业走向全球。

l未来可期,共创辉煌
“质量是医药行业的生命线,合规是国际化的基石。FDA的认证不是终点,而是我们迈向更广阔市场的新起点,”郭大海强调,“诺峰药业将继续坚持以最高标准推进质量管理、产能建设和合规运营,与更多优秀的行业伙伴共同推动中国医药全球化进程。”
诺峰药业将持续深化全球布局,加强创新研发与高质量生产,致力于为患者和医疗合作伙伴提供安全、有效、可信赖的药品。
质量铸就信任,合规通向全球。诺峰药业,将以FDA认证为新的起点,迈向更广阔的世界舞台!



